1924 aufgestellt, 2024 widerlegt: Chemiker haben eine Abweichung von der in vielen Chemie-Lehrbüchern stehenden Bredtschen Regel gefunden. Demnach gibt es doch stabile Doppelring-Kohlenwasserstoffe, die eine Doppelbindung an ihrem sogenannten „Brückenkopf“-Atom tragen – einem Atom zwischen den beiden Ringen. Möglich wird dieser Regelverstoß durch spezielle Reaktionswege und Helfer-Moleküle, wie das Team in „Science“ berichtet.
Kohlenwasserstoffe mit Doppelbindungen bilden die Basis vieler organischer Verbindungen – vom berühmten Benzolring über Nährstoffe und Arzneimittel bis hin zu vielen unserer Hormone. Im Normalfall bewirken die für diese Doppelbindungen typischen sp2- und π-Orbitale, dass die beteiligten Kohlenstoffatome gerade und in einer Ebene ausgerichtet sind. Moleküle, die von dieser Geometrie abweichen, sind eher selten und oft instabil.
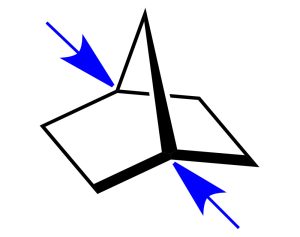
Julius Bredt und die „verbotene“ Doppelbindung
1924 fand der deutsche Chemiker Julius Bredt heraus, dass diese geometrischen Einschränkungen insbesondere für eine bestimmte Art von organischen Ringmolekülen gelten: In bicyclischen, aus nur zwei verbundenen Ringen bestehenden Kohlenwasserstoff-Molekülen darf die Doppelbindung nicht an einem sogenannten Brückenkopfatom stehen – den Kohlenstoffatomen, die an beiden Ringen beteiligt sind. Die entstehenden Spannungen verhindern die Bildung bicyclische Molekülen mit solchen „verbotenen“ Doppelbindungen.
„Bredts damalige Entdeckung führte zu der heute als Bredtsche Regel bekannten Regel, die sich in vielen Chemie-Lehrbüchern findet und auch von der International Union of Pure and Applied Chemistry (IUPAC) anerkannt ist“, erklären Luca McDermott und seine Kollegen von der University of California in Los Angeles. Demnach lassen einige wenige gegen diese Regel verstoßende Moleküle – sogenannte „Anti-Bredt-Olefine“ (ABO) – zwar künstlich herstellen, sind aber instabil.













